タンパク質の立体構造を解明することは、生命現象の理解や新薬開発において極めて重要です。
名城大学農学部の奥村裕紀教授(生物化学、分子細胞生物学)、スウェーデン・カロリンスカ研究所のLuca Jovine(ルカ・ヨヴィネ)教授、イギリス・ケンブリッジ大学のRandy J. Read(ランディ・リード)教授らの国際共同研究チームは、AIタンパク質構造予測ツール「AlphaFold」注1)を実験データの解析に直接統合する新手法「ROCKET」を開発しました。
本手法では、AIのニューラルネットワーク自体を実験データに適合(最適化)させることで、従来は手作業で行われていた補正を不要とし、高精度かつ高速な立体構造決定を可能にしました。さらに、低分解能の実験データに対しても、AIが有する事前知識(Prior / プライア)注2)を活用することで、高い信頼性を持つ分子モデルの構築が可能であることを示しました。
本技術は、構造生物学における解析プロセスの効率化と高度化を同時に実現するものであり、生命科学の基盤技術を刷新する技術として期待されます。
本研究成果は、2026年4月1日(日本時間)、英国の科学誌『Nature Methods』にオンライン掲載されました。
【ポイント】
・AIの知識を実験データ(X線結晶構造解析 注3)やクライオ電子顕微鏡 注4)など)の解釈プロセスに直接組み込む新技術を確立。
・タンパク質の機能・構造解析に深い知見を持つ奥村教授が共同研究に参加。AIによる予測と実際の実験データとの融合における検証に貢献。
・低分解能な実験データからでも、AIの事前知識を借りることで、極めて正確な分子モデルの構築が可能に。
【研究の背景】
タンパク質の立体構造を解明することは、生命現象の理解や新薬開発の鍵となります。近年、Google DeepMind社が開発した「AlphaFold」の登場により、アミノ酸配列から高精度な構造予測が可能になりました(2024年ノーベル化学賞受賞)。
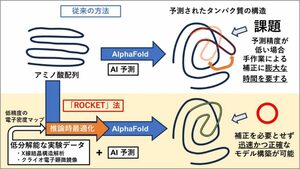
しかし、創薬研究などで必要とされる「原子レベルの厳密な確からしさ」を担保するには、依然としてX線結晶構造解析などの実験データ(電子密度マップ 注5))が不可欠です。従来のプロセスでは、AIの「予測モデル」をテンプレートとして使いつつ、実験データとの間に生じる細かな乖離を、研究者が膨大な時間をかけて手作業で修正・構築する必要がありました。この「予測」と「実測」の溝をどう埋めるかが、現代の構造生物学における大きな課題でした。
【研究内容及び本成果の意義】
本研究で開発した新手法「ROCKET」は、「推論時最適化(Inference-time optimization)」注6)という技術を導入した点に最大の特徴があります。その特徴は以下のとおりです。
1)AIと実験データを直接結びつける:
AlphaFoldの学習済みのニューラルネットワークを固定せず、実験で得られた電子密度マップに直接適合するように調整します。これにより、AIが学習した「化学的な妥当性(タンパク質として正しい形)」を維持したまま、実験データが示す「個別の事実」を反映したモデルを自動的に構築します。
2)低品質なデータからの構造解明:
実験データの質が低く、従来の手法では解釈が困難だったケースにおいても、AIの強力な「事前知識(Prior)」を借りることで、正確な構造決定が可能になります。
3)複雑な生体分子への応用:
奥村教授やJovine教授らが長年取り組んできた「受精に関わる複雑なタンパク質(ZP糖タンパク質など)」のような、解析が極めて困難な分子に対しても、本手法を用いることで迅速かつ正確なモデル構築が可能になります。
本成果の意義:
本手法の確立により、これまで数ヶ月を要していた難易度の高いタンパク質の構造決定が、数時間から数日へと劇的に短縮されます。これにより、感染症に対する迅速なワクチン開発や、がん治療における標的タンパク質の解析など、医療・ライフサイエンス分野に革命的な恩恵をもたらすことが期待されます。
【用語解説】
注1)AlphaFold(アルファフォールド):
Google DeepMind社が開発した人工知能(AI)によるタンパク質構造予測ツール。アミノ酸配列の情報から、そのタンパク質がどのような立体構造をとるかを極めて高い精度で予測し、構造生物学に革命をもたらした。
注2)事前知識(Prior / プライア):
統計学や機械学習の用語で、新しいデータを見る前にあらかじめ持っている情報の量や質のこと。本研究では、AlphaFoldが膨大なタンパク質データから学んだ「タンパク質として物理的に正しい形」という知識を、実験データの解析を助ける「ガイド」として活用している。
注3)X線結晶構造解析:
タンパク質の結晶にX線を照射し、その回折パターンを解析することで原子レベルの立体構造を決定する手法。創薬や生命現象の解明において最も信頼性の高い標準的な解析法の一つ。
注4)クライオ電子顕微鏡:
生体試料を急速凍結して自然に近い状態で観察し、コンピュータ解析で原子レベルの3D構造を再現する技術。タンパク質の結晶化が不要なため、創薬や生命科学の研究を飛躍的に進化させている。
注5)電子密度マップ:
X線結晶構造解析などの実験によって得られる、タンパク質分子内の電子の分布を示した3次元の地図。研究者はこのマップの中に原子のモデルを当てはめていくことで、正確な立体構造を決定します。
注6)推論時最適化(Inference-time optimization):
AIが学習済みの知識を使って答えを出す(推論)際に、手元にある特定のデータ(今回の場合は実験データ)に最も適合するように、AI内部の数値を微調整する技術。これにより、一般的な予測を「目の前の事実」に即した形へカスタマイズできる。
【掲載論文】
雑誌名:Nature Methods
タイトル:AlphaFold as a prior: experimental structure determination conditioned on a pretrained neural network
著者名:Alisia Fadini,Minhuan Li,Airlie J. McCoy,Suresh Banjara,Hiroki Okumura,Eve Napier,Pietro Fontana,Amir R. Khan,Luca Jovine,Thomas C. Terwilliger,Randy J. Read,Doeke R. Hekstra,Mohammed AlQuraishi
掲載日時: 2026年4月1日
DOI: https://doi.org/10.1038/s41592-026-03047-4
【研究体制】
本研究は、以下の複数の研究グループによる国際共同研究として実施されました。各研究グループの役割は、下記の3つに整理することができます。奥村教授の役割は、”2. 実験データの提供と検証” に含まれます。
理論・アルゴリズム開発
AIモデル(AlphaFold)を実験データと統合するための数学的フレームワークやプログラム開発を主導。(Randy J. Read教授:構造生物学、統計学の権威、Mohammed AlQuraishi助教授:AlphaFoldのオープンソース版 OpenFoldの開発者)
・University of Cambridge(イギリス・ケンブリッジ大学)
Cambridge Institute for Medical Research
Alisia Fadini (コロンビア大と兼任)・Airlie J. McCoy・Randy J. Read
・Columbia University(アメリカ・コロンビア大学)
Department of Systems Biology
Alisia Fadini (ケンブリッジ大と兼任)・Mohammed AlQuraishi
・Harvard University(アメリカ・ハーバード大学)
John A. Paulson School of Engineering and Applied Sciences / Dept. of
Molecular and Cellular Biology
Minhuan Li (フラットアイアン研究所と兼任)・Doeke R. Hekstra
2. 実験データの提供と検証
多様な生物学的サンプルとデータを提供し、開発した手法(ROCKETなど)によって得られる結果が生物学的な妥当性を有するかどうかの検証、および実際の実験データを用いた高度な解析・評価を実施した。
<受精メカニズムに関連するタンパク質を用いた検証>
・Umeå University(スウェーデン・ウメオ大学)
Department of Chemistry
Suresh Banjara
・Meijo University(日本・名城大学)
Department of Applied Biological Chemistry, Faculty of Agriculture(農学部応用生物化学科)
Hiroki Okumura(奥村裕紀)
・Karolinska Institutet(スウェーデン・カロリンスカ研究所)
Department of Medicine, Huddinge
Luca Jovine
<免疫系に関連するタンパク質を用いた検証>
・Trinity College Dublin(アイルランド・トリニティ カレッジ ダブリン)
School of Biochemistry and Immunology
Eve Napier・Amir R. Khan
・St. Jude Children’s Research Hospital(アメリカ・セントジュード小児研究病院)
Department of Immunology
Pietro Fontana
3. 計算基盤・ツール支援
(Thomas C. Terwiliger博士:構造解析ソフトPHENIXの開発者)
・Flatiron Institute(アメリカ・フラットアイアン研究所)
Center for Computational Mathematics
Minhuan Li
・Los Alamos(アメリカ・ロスアラモス国立研究所)
New Mexico Consortium
Thomas C. Terwiliger
【著者のコメント】
本論文では、AIによるタンパク質の立体構造予測の精度を大きく向上させる新手法「ROCKET」を開発しました。私たち自身も、タンパク質の結晶化やデータの質に制約され、構造決定に苦労してきましたが、本手法により、これまで十分に活用しきれなかった低分解能の実験データからでも、高精度な構造モデルを導けるようになりました。今後は「ROCKET」をさまざまな系に適用することで、タンパク質機能異常に起因する疾患の理解をさらに深め、新たな治療法の開発につながることを期待しています。
【本件に関するお問い合わせ先】
・研究内容に関すること
奥村裕紀
Tel: 052-838-2451
Email: hokumura@meijo-u.ac.jp
・広報担当
名城大学渉外部広報課
Tel: 052-838-2006
Email: koho@ccml.meijo-u.ac.jp
▼本件に関する問い合わせ先
名城大学渉外部広報課
住所:愛知県名古屋市天白区塩釜口1-501
TEL:052-838-2006
FAX:052-833-9494
メール:koho@ccml.meijo-u.ac.jp
【リリース発信元】 大学プレスセンター https://www.u-presscenter.jp/